 環境技術解説
環境技術解説
排煙脱硫技術とは、石炭火力発電所などの排ガスから硫黄酸化物(SOx)を除去する技術で、アルカリ水溶液やスラリーでSO2を吸収する「湿式」や、活性炭等を用いる「乾式」などがある。火力発電所等における大量処理から小規模工場プラントでの処理まで、化石燃料を燃焼する施設で設置され、規模やコスト、副産物の種類と用途等によって様々なプロセスが選択されている。
日本が戦後急速に産業の復興を成し遂げる中で、全国の工場からの硫黄酸化物の排出量が増大し、四日市ぜんそくをはじめとする大気汚染が深刻化した。そうした流れの中で、硫黄酸化物に対する規制が設けられ、順次強化された。排煙脱硫装置は、このような規制をクリアし、日本の産業の発展を支えるのに貢献する技術として実用化が進んだ。現在では、石炭火力発電所をはじめ、廃棄物焼却炉など化石燃料等を使用する各種の事業所に導入されている。
また、中国をはじめとするアジアでは工業化の進展にともなって硫黄酸化物の排出増加が見込まれていることから、排煙脱硫装置はアジア各地の公害対策と広域的な酸性雨問題の解決に寄与すると期待される。

排煙脱硫装置全景
写真提供:三菱重工業(株)
※外部リンクは別ウィンドウで表示します
硫黄酸化物(SOx)は、石炭、石油など硫黄分を含む燃料の燃焼にともない発生し、慢性気管支炎などの原因となることが知られている。硫黄酸化物には、二酸化硫黄(SO2)のほか、一酸化硫黄(SO)、三酸化硫黄(SO3)などが含まれる。法律上は二酸化硫黄に対する環境基準が設定されているが、ここでは、二酸化硫黄を中心に硫黄酸化物全般について記述する。
硫黄酸化物は、日本では古くから代表的な大気汚染物質とされてきた。昭和30年代から40年代にかけての高度成長期には、十分な排ガス処理装置が設置されていなかったため、全国の工業地帯で硫黄酸化物が大量に排出され、四日市ぜんそくをはじめとする大気汚染問題を引き起こした。
(1)濃度規制からK値規制へ
硫黄酸化物(二酸化硫黄)の規制については、はじめは煤塵(ばいじん)とともに「ばい煙」として規制対象となってきた。最初に硫黄酸化物に対する規制が盛り込まれたのは、昭和38年に施行された「ばい煙の排出の規制等に関する法律」で、この中に火力発電所等のばい煙発生施設の排出口における排出濃度の規制が設定された。
しかし、人の健康保護の観点からは、硫黄酸化物の地上濃度が重要になることから、昭和43年に施行された大気汚染防止法(大気汚染の防止に関する法律)では、いわゆる「K値規制」が採用された。
K値規制は、各ばい煙発生施設の煙突の高さ(実際には煙突の高さだけでなく、排出速度、ガスの排出温度等を考慮して補正)と排出量から算出される硫黄酸化物の最大着地濃度にもとづいて、施設ごとの1時間の硫黄酸化物排出量の上限を定めるものである。K値はこのときの計算に用いられる定数で、地域ごとに設定され、値が小さいほど厳しい基準となる。
なお、大気汚染防止法は、昭和45年のいわゆる「公害国会」において改正が行われ、都道府県による上乗せ規制の導入や、指定地域での規制から全国規制への拡大など、規制が強化された。
(2)規制のさらなる強化(総量規制方式)
硫黄酸化物規制がK値規制に移行し、強化されたことにともない、昭和40年代後半には硫黄酸化物による大気汚染は改善された。しかし、それでも工場密集地域においては不十分な状況が続いていた。そこで、昭和49年の大気汚染防止法の改正では、諸外国に先駆けて「総量規制方式」が導入された。これは、一定の範囲の地域における大気汚染物質の総量の許容濃度を環境基準に照らして科学的に算定し、これ以下に排出量を抑えるように個別発生源の規制を行う方式である。
硫黄酸化物対策としては、燃料中の硫黄分を低減することが第一の対策となる。原油については、低硫黄の原油の輸入、原油脱硫(燃料として使用する前の原油から化学的なプロセスにより硫黄を除去する方法)が公害対策として進められた。石炭についても、高硫黄の石炭から低硫黄の石炭への転換、燃焼前の石炭からの硫黄分の除去が行われた。
燃焼後の排ガスから硫黄酸化物を除去する技術である排煙脱硫技術は、このような硫黄酸化物対策技術の1つとして位置づけられ、硫黄酸化物規制の強化にともなって広く実用化されるようになった。
排煙脱硫装置の本格的な開発が始まったのは、公害問題が顕在化し始めた1960年代前半からで、大型火力発電所向けの排煙脱硫装置の開発が中心であった。特に、1966年には、工業技術院が大型プロジェクトの1つとして「乾式法」による排煙脱硫を取り上げ、脱硫率90%を目標に民間委託による研究開発が行われた。その結果、1960年代には乾式法を中心に様々な国産排煙脱硫技術が開発され、その数は約50種に達したといわれる。世界的に見ても、日本で開発された排煙脱硫技術のレベルは高いといわれている。
排煙脱硫装置の本格的な実用化は昭和49年(1974年)の硫黄酸化物の総量規制の導入が契機となった。その際、「石灰-石膏法」が採用されることが多く、1980年以降のほとんどすべての事業用火力発電所には、石灰-石膏法が採用されてきた。以降、排煙脱硫装置のメーカーは石灰-石膏法を基礎にしながら、その合理化研究等を行っている。
現在、日本では排煙脱硫設備の設置も行き渡っているが、今後、中国や東南アジア地域でのニーズが拡大することが確実である。そのため、排煙脱硫メーカーの多くは、近年では海外市場に適用した技術開発を意識しており、途上国に適した運転が容易で、低価格な、簡易脱硫装置の開発が進められている。
また、近年では、脱硫性能のみならず、微細ばいじんや、窒素酸化物を同時に除去できる技術に対するニーズも高まっている。
わが国の硫黄酸化物対策の進捗状況を図1に示す。二酸化硫黄濃度の年平均値は、一般局(一般環境大気測定局)、自排局(自動車排出ガス測定局)とも昭和45頃から大幅に改善され、近年は0.04ppm程度で推移している。環境基準の達成率は、平成17年度で一般局99.7%、自排局100%と、良好な状態が続いている。
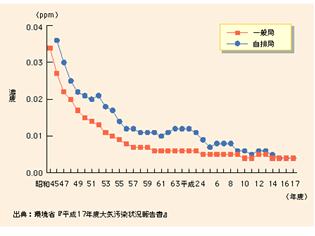
図1 二酸化硫黄濃度の年平均値の推移(昭和45年度~平成17年度)
出典:平成19年版環境・循環型社会白書(環境省)
http://www.env.go.jp/policy/hakusyo/h19/html/hj07030201.html#3_2_1_4
1960年代~70年代にかけて、硫黄酸化物は地域の公害問題の原因としてとらえられていたが、1980年代後半になると酸性雨の原因物質として、広域的な環境問題の視点から注目されるようになった。
実際、日本で観測される硫黄酸化物の主な排出源は、中国の工場等といわれている。東アジアは中国をはじめとして今後の経済発展が見込まれており、硫黄酸化物の排出量がさらに増加すると考えられることから、今後も硫黄酸化物のモニタリングを続けることが重要である。
排煙脱硫装置が必要とされる分野は、化石燃料等を燃焼する施設であり、火力発電所、紙・セメント製造工場、廃棄物焼却炉等が挙げられるが、最も大きな処理量を求められるのは火力発電所向けの排煙脱硫装置である。図2に示す通り、装置の総処理能力で見ると、電気業(火力発電所)が全体の半分以上を占めている。
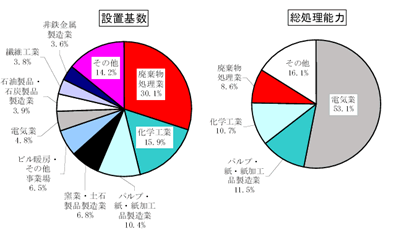
図2 排煙脱硫装置の業種別の設置数・処理能力
出典:環境省「平成16年度大気環境に係る固定発生源状況調査」
http://www.env.go.jp/air/osen/kotei/h16.pdf
排煙脱硫プロセスは、大別して「湿式法」「乾式法」および「半乾式法」に分類され、現状では湿式法の採用実績が圧倒的に多い。特に火力発電所向けの、大容量排ガス処理プロセスとしては、湿式法の1つである「石灰-石膏石膏法」が世界の主流となっている。代表的な排煙脱硫プロセスを表1に示す。
| プロセス名 | プロセスの概要 | 実用化状況 | |
|---|---|---|---|
| 湿式法 | 石灰-石膏法 | ・ SO2をアルカリ水溶液またはスラリーで吸収 ・ 生成する亜硫酸塩を必要に応じて酸化し硫酸塩に添加 ・ 生成物は、回収利用または廃棄 ・ 生成する亜硫酸塩を分解して高濃度のSO2ガスに転換し、硫酸等を回収するプロセスも提案されている ・ 使用するアルカリの種類により幾つかのプロセスがある。 | 大~中規模プラントで実績多 |
| 水酸化マグネシウム法 | 小規模プラントで実績多 | ||
| ソーダ法 | ガラス、パルプ産業や小規模プラントに適用 | ||
| 乾式法 | 活性炭吸着法 | ・ 活性炭によりSO2を吸着 ・ 吸着SO2を加熱脱着して高濃度SO2を回収し、硫酸、硫黄等に転化 | 一部で運転中 |
| 電子ビーム法 | ・ アンモニア存在下で電子ビームを照射 ・ 生成物を集じん装置で捕集 | 過去に実証試験を実施 | |
| 石炭灰利用法 | ・ 石炭灰、水酸化カルシウム、使用済み吸収剤を混合したペレットを吸収剤として利用 ・ 石炭灰の有効利用方策も兼ねる | 石炭火力発電の比率の高い北海道で研究が進められ、道内で1基が稼働中 | |
| 炉内脱硫法 | ・ 流動床ボイラーの流動媒体に石灰石を使用して炉内で脱硫を行う ・ 石灰石を石炭と混合して高温の炉内でSO2を除去 | 国内外の発電所の加圧流動床ボイラーで採用 | |
| 半乾式法 | スプレードライ法 | ・ 消石灰スラリーを反応塔中に噴霧してSO2を亜硫酸カルシウム等の粉体に転化 ・ 集じん装置で捕集、捕集物は廃棄 | 欧米で実績多数 |
出典:『環境汚染防止のための環境技術・装置大事典』(産業調査会,2003年2月)をもとに作成
(1)【湿式】石灰-石膏法
アルカリ成分である石灰石(CaCO3)をスラリー状にして吸収塔内でSO2と反応させ、SO2を吸収するとともに、副生物として石膏を回収する方式である。反応式は以下のように表される。石灰石が安価であること、副生物である石膏を回収して販売できることから、火力発電所など大型ボイラで採用されている(図3)。
SO2+CaCO3+0.5H2O→CaSO3・0.5H2O + CO2(吸収反応式)
CaSO3・0.5H2O+0.5O2+1.5H2O → CaSO4・2H2O (酸化反応式)
具体的なプロセスとしては、排ガスに吸収液を噴霧(スプレー)してSO2と反応させるスプレー方式や、グリッド状の充填物の表面に吸収液を流すグリッド方式などが採用されている(図3の装置ではグリッド方式が採用されている)。吸収反応の次段階である酸化反応を吸収塔の外で行う「酸化塔別置方式」と吸収塔の中でそのまま行う「吸収塔内酸化方式」とがある(図4)。設備が簡単な吸収塔内酸化方式が主流で、この方法では、吸収塔タンクの下部に直接空気を吹き込むことによって吸収塔で吸収したSO2を全量石膏に転換する。

図3 排煙脱硫装置全景
写真提供:三菱重工業(株)
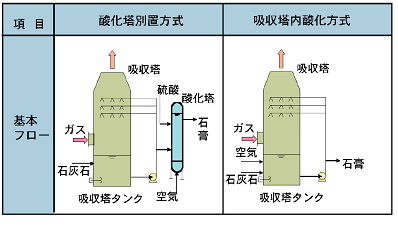
図4 石灰-石膏法の概要
出典:(独)新エネルギー・産業技術総合開発機構・(財)石炭エネルギーセンター「日本のクリーン・コール・テクノロジー(5B1. SOx処理技術)」
http://www.brain-c-jcoal.info/cctinjapan-files/japan/2_5B1.pdf
水を使用する湿式共通の課題として、用水の確保と排水の処理が挙げられる。石灰-石膏法において、水は、石灰石のスラリー化による吸収液製造、装置内部の洗浄等に必要である。脱硫装置出口の排ガスは水分の蒸発のために大量の水分を含んでいることから、これを間接冷却して凝縮水を得て水使用量を低減する開発が進められている。また、副生石膏を回収した後の排水には塩素系化合物やばいじん等が含まれているが、これらを固化処理して排水を出さないようにした無排水システムも開発されている。
また、中国をはじめとするアジア地域向けの脱硫装置については、簡易で低コストな脱硫装置の開発が進められており、排ガス煙道や煙突下部に組み込む形の脱硫装置が開発・実用化されている。
(2)【湿式】水酸化マグネシウム法
石灰-石膏法では石膏回収工程や排水処理工程が複雑になるため、小型ボイラーへの適用には向かない。そこで、小規模プラントでは、石灰に次ぐ安価なアルカリである水酸化マグネシウムを用いた「水酸化マグネシウム法」が多く採用されている。
水酸化マグネシウム法のフローは、回収工程を除けば石灰-石膏法とほぼ同様である。この方式による脱硫後の副生物は水溶性の硫酸マグネシウムであるため、石灰-石膏法のような回収工程は不要になり、設備が簡素化できる。また、原料の水酸化マグネシウムはスラリー状のままタンクローリーで供給される。吸収反応・酸化反応は以下の通りである。
SO2 + Mg(OH)2 → MgSO3 + H2O (吸収反応式)
SO2 + MgSO3 + H2O → Mg(HSO3)2 (吸収反応式)
MgSO3 + 0.5O2 → MgSO4 (酸化反応式)
(3) 【湿式】ソーダ法
吸収剤として、苛性ソーダ(NaOH)又は炭酸ソーダ(Na2CO3)を使用し、SO2と反応させて亜硫酸ナトリウム(Na2SO3)を生成させる。Na2SO3は、紙パルプの蒸解用にそのまま利用できる。このほか、Na2SO3を酸化して硫酸ナトリウム(Na2SO4)とし、そのまま放流する方式などがある。
ソーダ法は、1960年代後半にパルプ工場や小規模設備で用いられたが、吸収剤の苛性ソーダが高価で運転費が高くなることから、より安価な吸収剤である水酸化マグネシウムを用いる方法に取って代わられている。
(4)【乾式】活性炭吸着法
活性炭によってSO2を回収する本法は、脱硫単機能ではなく、同時脱硫・脱硝技術として、また、ダイオキシン除去や、重金属元素の除去等の他成分の除去機能を持つ技術として、既に国内火力発電所等に適用されている(図5)。

図5 活性炭脱硫装置
出典:(独)新エネルギー・産業技術総合開発機構・(財)石炭エネルギーセンター「日本のクリーン・コール・テクノロジー(5B3. 同時脱硫脱硝技術)」
http://www.brain-c-jcoal.info/cctinjapan-files/japan/2_5B3.pdf
活性炭吸着法は、吸着塔、脱離塔、活性炭循環移送装置からなる。発生源からの排ガスには、アンモニアが添加されて吸着塔に導入され、活性炭上で以下の反応により硫酸またはそのアンモニウム塩として吸着される。
SO2 +0.5O2 + H2O → H2SO4※
H2SO4 + NH3 → NH4HSO4※
※は吸着状態
なお、NOx等他成分の吸着も行う場合には複数の活性炭セルからなるモジュールで吸着塔を構成し、各モジュールを通過しながら排ガス中の各成分の除去が行われる。
吸着塔でSOx等を吸着した活性炭は脱離塔に送られ、350℃以上に加熱、以下の反応で再生される。再生した活性炭は冷却部で150℃以下に冷却された後、ダストをふるい分け分離し、吸着塔で再び使用される。一方、回収した濃縮SO2ガスは洗浄精製した後、酸化、または還元されて最終的には硫酸や単体の硫黄等として回収される。
H2SO4※ + 0.5C → SO2 + 0.5CO2 + H2O NH4HSO4※ +0.5C-O(表面酸化物) → SO2 + 0.5N2 +2.5H2O ※は吸着状態
(5)【乾式】電子ビーム法
排ガス中のNOxとSOxと吹き込んだアンモニアに電子ビームを照射して反応させ、微粒の硫酸アンモニウムや硝酸アンモニウムにし、これらを集じん機で回収する方式である。副産物の硫酸アンモニウム等は肥料として使用できる(図6)。
排水処理が不要で、硫酸アンモニウムを肥料として利用できるメリットはあるが、電子ビームを発生させる特殊な設備が必要であることから、実証試験段階にとどまっている。
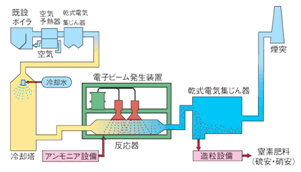
図6 電子ビーム法脱硫プロセス
出典:(独)新エネルギー・産業技術総合開発機構・(財)石炭エネルギーセンター「日本のクリーン・コール・テクノロジー(5B3. 同時脱硫脱硝技術)」
http://www.brain-c-jcoal.info/cctinjapan-files/japan/2_5B3.pdf
(6)【乾式】石炭灰利用法
石炭灰の有効利用の一環として開発された技術で、石炭灰と水酸化カルシウム、使用済みの吸収剤から新規に吸収剤を製造し、この吸収剤を用いて排ガス中のSOxを除去する方式である(図7)。
3つの原料を混練してペレットを造粒し、これらを吸収塔に充填して排ガス中のSOxと接触させてSO2の固定化を行う。石炭灰は直接SO2を吸収するわけではないが、脱硫率向上に効果がある。また、脱硝、集じん効果もある。石炭火力発電の比率の高い北海道で研究が進められ、道内の発電所で1基が稼動している。
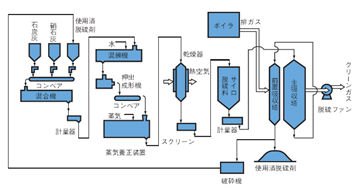
図7 石炭灰利用法の概要
出典:(独)新エネルギー・産業技術総合開発機構・(財)石炭エネルギーセンター「日本のクリーン・コール・テクノロジー(5B1. SOx処理技術)」
http://www.brain-c-jcoal.info/cctinjapan-files/japan/2_5B1.pdf
(7)【乾式】炉内脱硫法
流動床ボイラーの流動媒体に石灰石を使用することにより炉内で脱硫する方法であり、設備を大幅に簡略化できる経済的な手法である。脱硫用の石灰石は石炭と混合し、炉内温度760~860℃でSO2の除去を行う。国内外の発電所の加圧流動床ボイラーで採用されている。
(8)【半乾式】スプレードライ法
半乾式法と呼ばれ、生石灰に水を加えて消石灰スラリーをつくり、スプレードライヤー内に噴霧して排ガス中のSO2とCa(OH)2を反応させて除去する方法。副生物は石膏や亜硫酸ガスの混合粒子となり、廃棄物として処理される。スプレー式の石灰-石膏法と似たプロセスであり、欧米で実績が多い。
近年、硫黄酸化物は酸性雨の原因として注目されており、中国等で発生する硫黄酸化物の日本への影響についての研究が行われている。
日本で観測される酸性雨は、工場などの脱硫システムが高度に発達しているため、硫黄酸化物(SOx)による硫酸系の寄与割合が他の国などの酸性雨に比べて低く、自動車から排出される窒素酸化物(NOx)による硝酸系の寄与割合が高い。しかし、日本海側では冬季の硫酸塩の沈着量が夏季より多いことが知られている。これらは、硫黄酸化物がアジア大陸から冬の季節風に乗って飛来したと考えられて、その原因は中国等からの排出と考えられている。
現在、(独)国立環境研究所では、アジアの広域的な大気環境問題を解決するため、東アジアにおける発生源インベントリーの整備などの研究を進めている。アジアの経済発展による化石燃料使用の増加にともない、硫黄酸化物の発生量はますます増加すると予想されており(図8)、アジア各国からの硫黄酸化物排出と日本の酸性雨との因果関係の研究が重要になっている。
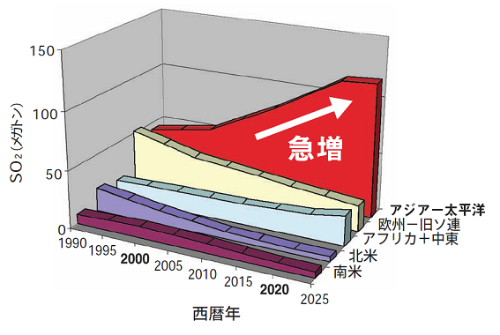
図8 化石燃料使用量の増加によるSO2発生量の予測
出典:国立環境研究所 環境儀No.12
http://www.nies.go.jp/kanko/kankyogi/12/02-03.html